Deux publications récentes mettent en cause l'étude de bioéquivalence qui a permis à Merck de remplacer l'ancienne formule du Levothyrox par la nouvelle en 2017. Les moyennes obtenues lors de cette étude masqueraient la réalité des situations individuelles.
En France, environ 2,5 millions de personnes prennent de la lévothyroxine, en grande majorité sous la forme de Levothyrox. Une nouvelle formule de ce médicament est arrivée dans les pharmacies en mars 2017. Seuls les excipients changeaient, le lactose de l'ancienne formule étant remplacé par le mannitol et l'acide citrique. Ce changement de formule a été justifié par le souci d'avoir une meilleure stabilité du produit.
Suite à l'arrivée du nouveau Levothyrox, des milliers de patients ont déclaré des effets secondaires. L'affaire est même arrivée devant la justice, avec une action collective au tribunal de Lyon, mais les plaignants ont été déboutés de leur demande. En parallèle, l'ANSM a considéré que seul 1,43 % des patients avaient déclaré des effets secondaires.
Cependant, les travaux d'une équipe franco-britannique semblent donner raison aux patients. Ils ont fait l'objet de deux publications scientifiques. Les chercheurs des universités de Toulouse et de Londres se sont intéressés à l'étude de bioéquivalence réalisée par Merck pour savoir si l'ancienne et la nouvelle formule du Levothyrox étaient interchangeables. Avant de commencer un traitement avec la lévothyroxine, un dosage des hormones thyroïdiennes est généralement préconisé pour estimer la bonne dose de médicament nécessaire. Si les deux formules de Levothyrox sont bien équivalentes, alors les patients peuvent passer de l'une à l'autre sans problème.
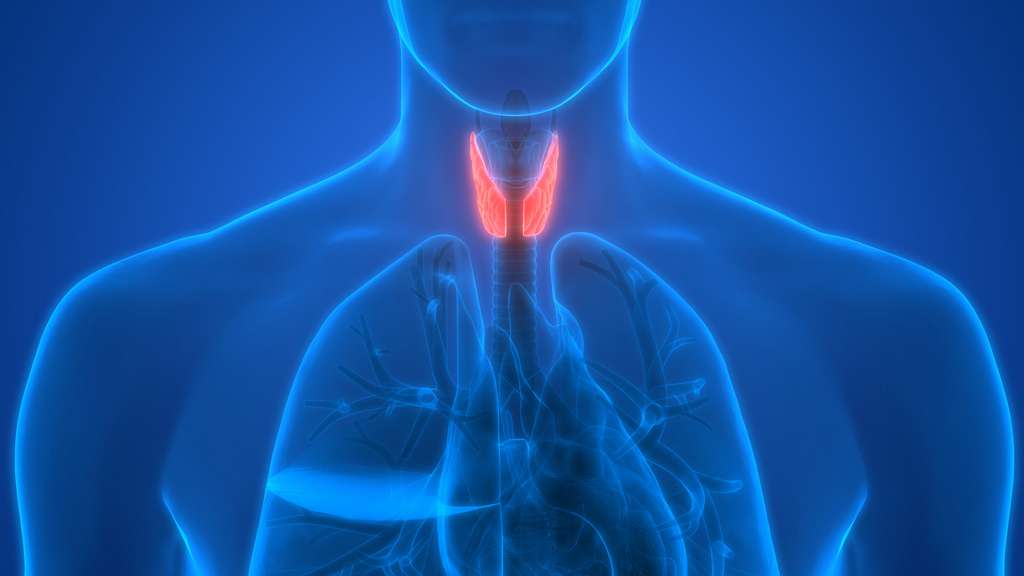
La thyroïde est un organe qui produit des hormones. Le Levothyrox vise à compenser un déficit en hormones thyroïdiennes. © magicmine, Fotolia
Les moyennes cachent des situations individuelles problématiques
L'étude de bioéquivalence a inclus 204 personnes en bonne santé, âgées de 18 à 50 ans (59 % d'hommes). Pour savoir si les deux formulations étaient équivalentes, les volontaires ont pris une des deux formules, l'ancienne ou la nouvelle, et les variations de l'hormone ont été mesurées dans le sang. Plus tard, les scientifiques ont testé l'autre formule pour comparer et sont arrivés à la conclusion que l'ancien médicament pouvait être remplacé par le nouveau.
Un premier article paru dans la revue Clinical Pharmacokinetics a critiqué cette étude de Merck. En effet, les auteurs relèvent que chez plus de la moitié des participants, la bioéquivalence du produit n'était pas établie : le caractère substituable du médicament n'est donc pas démontré chez eux !
Plusieurs hypothèses pourraient expliquer que certaines personnes développent des effets secondaires. Par exemple, chez les patients, l'absorption du médicament peut être différente par rapport à des sujets en bonne santé. De plus, le mannitol, excipient présent dans la nouvelle formule et absent de l'ancienne, influencerait la fonction intestinale et donc la biodisponibilité de la lévothyroxine.
Dans un nouvel article paru cette semaine, la même équipe s'interroge sur le fait que Merck ait inclus plus de 200 personnes dans cette étude. En effet, ce type d'étude de bioéquivalence se réalise souvent sur bien moins de sujets. Or d'après Pierre-Louis Toutain, un des auteurs de cette recherche, plus le nombre de participants est important, plus il est facile d'obtenir un résultat qui entre dans l'intervalle de confiance fixé (0,9-1,1) : « Si on avait pris un nombre classique de sujets (entre 24 et 48, mais pas 200), ce ne serait pas passé. » L'intervalle de confiance donne un degré de sûreté du résultat. Un intervalle de confiance restreint à 0,9-1,1 semble assurer une certaine sécurité du résultat, mais ce choix « est annulé par le fait que l'on prend beaucoup de sujets ».
- Avant le changement de formule de Levothyrox, Merck a réalisé une étude de bioéquivalence sur plus de 200 personnes.
- Une équipe franco-britannique signale que dans cette étude le médicament n’était pas substituable chez plus de la moitié des sujets.
- Les études de bioéquivalence sont généralement réalisées sur des échantillons plus petits.
Source : Levothyrox : polémique autour de la bioéquivalence de la nouvelle formule
Articles en Relation

Comment pose-t-on un diagnostic en médecine ?
Image de freepik
Image de gpointstudio sur Freepik
Comment pose-t-on un diagnostic en médecine ?
Yves Hansmann, Université de Stra...

Le sport booste la mémoire jusqu’à 24 heures après la séance - nouvelle recherch...
Image de freepik
Image de freepik
Le sport booste la mémoire jusqu’à 24 heures après la séance - nouvelle recherche
Mikaela Bloomb...

Un savon inventé par un ado pourra-t-il un jour traiter le cancer de la peau ? C...
Image de freepik
Image de freepik
Un savon inventé par un ado pourra-t-il un jour traiter le cancer de la peau ? Ce que dit la science
...

Apports en vitamine D par le soleil, les aliments et la supplémentation : mythes...
Image de freepik
Image de freepik
Apports en vitamine D par le soleil, les aliments et la supplémentation : mythes et réalités
M. Ca...

Sommeil : comment la caféine trompe notre cerveau
Image de freepik
Image de gpointstudio sur Freepik
Sommeil : comment la caféine trompe notre cerveau
Armelle Rancillac ????, Inse...

Cataracte : vous craignez de vous faire opérer ? Voici ce qu’il faut savoir
Image de freepik
Image de freepik
Cataracte : vous craignez de vous faire opérer ? Voici ce qu’il faut savoir
Allan Steigleman...